有关过氧化钠与二氧化碳、水的反应
1、反应原理
2Na2O2+2CO2=2Na2CO3+O2
2Na2O2+2H2O=4NaOH+O2↑
2、重要关系
(1)电子转移关系:
在Na2O2与CO2或H2O的反应中,Na2O2既作氧化剂又作还原剂,每生成1 mol O2都转移2 mol电子。
(2)物质的量的关系:
无论是CO2或H2O的单一物质还是二者的混合物,通过足量的Na2O2时,CO2或H2O与放出O2的物质的量之比均为2∶1。
(3)气体体积关系
无论是CO2或H2O(g)的单一物质还是二者的混合物,通过足量的Na2O2时,气体减小的体积或原混合气体体积的一半等于生成O2的体积。
(4)固体质量关系:
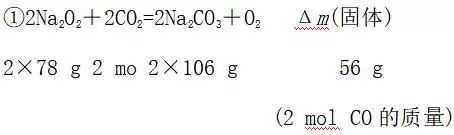
即:发生反应①时,固体增加的质量等于与CO2等物质的量的CO的质量。

即:发生反应②时,固体增加的质量等于与H2O等物质的量的H2的质量。
(5)先后顺序关系:
一定量的Na2O2与一定量的CO2和H2O(g)混合物的反应,可看做Na2O2先与CO2反应,待CO2反应完成后,Na2O2再与H2O发生反应。
相关文章
推荐内容
教育新鲜事
 高二化学||化学反应速率
高二化学||化学反应速率 3大技巧让你高考化学选
3大技巧让你高考化学选 高考化学必备元素周期表
高考化学必备元素周期表 高中化学实验现象80例,
高中化学实验现象80例,